
HEALTH FOOD
保健食品
国产保健食品研发申报流程
发布时间:
2017-11-27 14:34
来源:
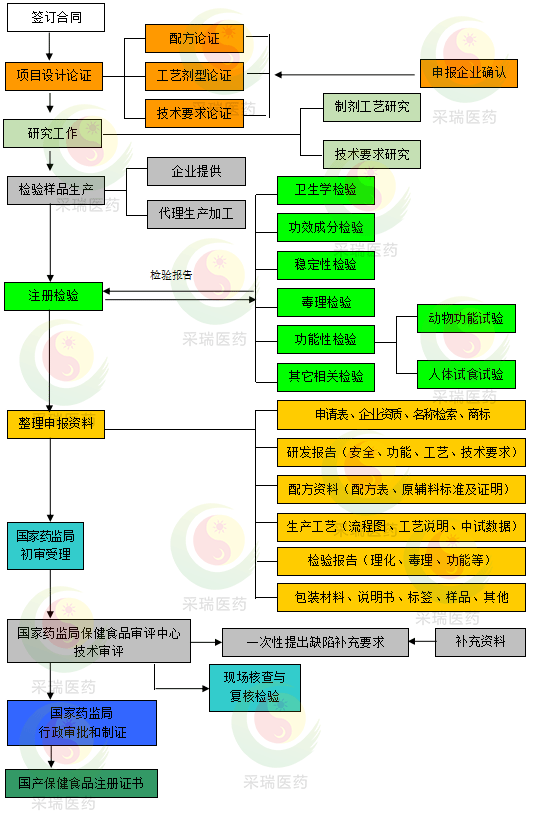
流程简图
⇅

【国产保健食品研发申报流程说明】
采瑞公司根据自身多年来的工作经验和管理模式,将保健食品研究开发和申报注册过程分为六个阶段,具体如下。
◖第一阶段:前期研究论证阶段◗
在委托公司的配合下,主要由采瑞公司完成,根据需要召开专家咨询论证会,确定最后开发方案。
1、配方研究和论证:配方所有原料必须符合国家食品药品监督管理总局的法律法规要求,每个原料的用量必须合适,量太多不符合安全性要求,量太少不不符合功能性要求。所有原料必须具有与申报功能相关的科学文献支持。配方中各个原料之间要有合理的配伍关系,并符合生产工艺的要求,能够制成成品,且符合技术要求。
2、工艺研究:根据初步配方选择适宜的辅料进行制剂研究。研究的最终制剂的相关技术参数应符合要求,如外观、硬度、脆碎度、崩解度、均匀度等。另外,产品灭菌工艺尤其值得关注。产品的生产工艺必须具有大生产规模的可行性和合理性。
3、技术要求研究:包括常规指标和功能性(标志性)指标。常规指标包括微生物(细菌、霉菌和致病菌)、重金属、农药残留、水分、灰分、净含量、崩解度、颗粒度、及其他限制性指标等。功能性(标志性)指标包括线性、精密度、回收率、检出限等研究,指标需根据配方制定,比如,总黄酮、总皂苷等。
◖第二阶段:样品加工阶段◗
在具有保健食品生产资质(GMP认证)的企业完成样品加工。含原辅料包材自检、成品自检等。按照检验要求提供中试规模大生产的连续三批足量合格的样品。
◖第三阶段:检验阶段◗
将检验用样品送到国家认定的检验机构进行相关检验。
1、理化类检验:包括卫生学、功效(标志性)成分、稳定性试验。稳定性试验分加速稳定性试验和长期稳定性试验。益生菌类产品需要进行长期稳定性试验。
2、毒理试验:五项,急性毒性试验、小鼠精子畸形试验、小鼠骨髓微核试验、Ames试验、30天喂养试验。
3、功能试验:增强免疫力、缓解体力疲劳等功能,只需做动物功能试验;缓解视疲劳、祛黄褐斑等功能,只需做人体试食试验;抗氧化、辅助降血糖、辅助降血脂、减肥等功能,需要做动物功能试验和人体试食试验。缓解体力疲劳、减肥、促进生长发育功能,还需要做兴奋剂检验。
◖第四阶段:初审受理阶段◗
国家药监局对申报资料进行形式审查,申报资料合格后正式受理,提供产品受理通知书。
◖第五阶段:国家审评阶段◗
保健食品审评中心组织保健食品审评专家对申报资料进行技术审评,发放审评意见通知书,由企业提供相关补充资料及说明,技术审评完成后,根据需要进行现场核查和复核检验。
◖第六阶段:行政审批和制证阶段◗
国家食品药品监督管理总局对产品进行行政审批和制证。
上一页
下一页
上一页
下一页
-
地址:北京市朝阳区惠新西街18号罗马花园B座201室
邮编:100029
电话:010-64286750
热线:400-080-1918
-
咨询电话:
010-64286750 (科研热线)
010-64215652 (销售热线)

采瑞医药

采瑞健康
采瑞成立20年、专注于保健食品研究开发、申报注册相关项目!
